For nylig udgav FDA de endelige retningslinjer for liste over kosmetiske faciliteter og produkter og lancerede en ny kosmetikportal kaldet 'Cosmetic Direct'. Og FDA annoncerede obligatoriske krav til registrering af kosmetiske faciliteter og produktliste fra den 1. juli 2024 for at sikre, at regulerede virksomheder har tilstrækkelig tid til at forberede og indsende oplysninger.
1. Bestemmelser
1)Modernization of Cosmetics Regulation Act of 2022, (MoCRA)
2)Federal Food, Drug and Cosmetic Act (FD&C Act)
3) Fair Packaging and Labeling Act (FPLA)
2. Anvendelsesområde
Ifølge amerikansk lovgivning defineres kosmetik som genstande, der påføres, spredes, sprøjtes eller på anden måde bruges på den menneskelige krop for at rense, forskønne, forbedre tiltrækningskraften eller ændre udseende.
Specifikt omfatter det hudfugtighedscreme, parfume, læbestift, neglelak, øjen- og ansigtskosmetik, rengøringsshampoo, permanent, hårfarve og deodorant, samt ethvert stof, der bruges som kosmetisk ingrediens. Sæbe hører ikke til kosmetik.
3. Klassifikation
Ifølge MoCRA klassificerer den amerikanske kosmetik-FDA kosmetik i følgende kategorier:
-Babyprodukter: inklusive babyshampoo, hudpleje talkum, ansigtscreme, olie og væske.
-Badeprodukter: inklusive badesalt, olie, medicin, skummiddel, badegel mv.
- Øjenkosmetik: såsom øjenbrynsblyant, eyeliner, øjenskygge, øjenskyl, øjenmakeupfjerner, øjensorte osv.
Kosmetik med specielle effekter, såsom anti-rynke, blegning, vægttab osv., skal samtidig registreres som håndkøbsmedicin. Det skal bemærkes, at disse nye regler gælder for kosmetik, der eksporteres til det amerikanske marked.
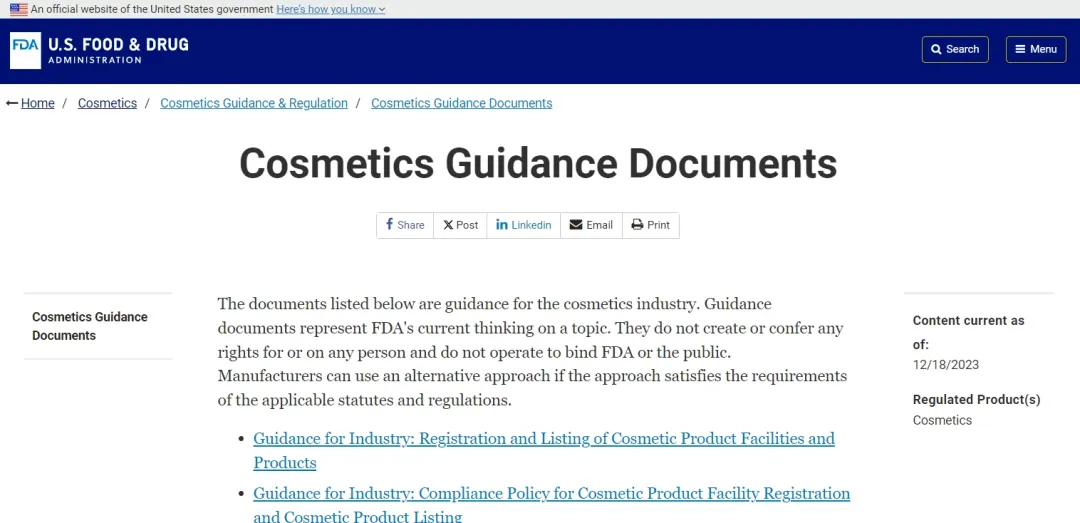
FDA registrering
MoCRA har ikke kun tilføjet følgende nye krav, herunder etablering af kosmetikansvarlig person-systemet, obligatorisk indberetning af alvorlige bivirkninger, overholdelse af Good Manufacturing Practice (GMP), fabriksregistrering og produktlisteregistrering, tilvejebringelse af tilstrækkelige sikkerhedscertifikater, men krævede også, at etiketten var mærket med den ansvarlige personoplysninger, essensallergener, professionel brug af produkterklæringer, udvikling og frigivelse af asbestdetektionsmetoder i kosmetik, der indeholder talkum, og sikkerhedsrisikovurderingen og dyreudfasningstesten af PFAS i kosmetik.
Forud for implementeringen af MOCRA kan kosmetikproducenter/-pakkere registrere deres fabriksfaciliteter hos FDA gennem US FDA's Voluntary Cosmetic Registration Program (VCRP), og FDA har ikke obligatoriske krav til dette.
Men med implementeringen af MOCRA og den kommende obligatoriske deadline skal alle virksomheder, der sælger kosmetik i USA, registrere deres produktionsfaciliteter hos FDA og opdatere deres registreringsoplysninger hvert andet år, herunder navn, kontaktoplysninger osv. Faciliteter beliggende uden for USA Stater er også forpligtet til at give oplysninger og kontaktoplysninger for agenter i USA. Der er også nogle supplerende oplysninger, der skal udfyldes, såsom moderselskabsoplysninger, virksomhedstype, emballagebilleder, produktwebsidelinks, om det er en professionel kosmetik, den ansvarliges Dun&Bradstreet-kode osv. Det er ikke obligatorisk at udfylde i. Eksisterende kosmetiske faciliteter skal registreres hos FDA inden for et år efter, at de nye regler er udstedt, og registreringsperioden for nye kosmetiske faciliteter er inden for 60 dage efter, at de er involveret i kosmetik forarbejdning og produktion.
BTF Testing Lab, vores virksomhed har laboratorier for elektromagnetisk kompatibilitet, sikkerhedsforskrifter Laboratorium, trådløst radiofrekvenslaboratorium, batterilaboratorium, kemisk laboratorium, SAR-laboratorium, HAC-laboratorium osv. Vi har opnået kvalifikationer og autorisationer såsom CMA, CNAS, CPSC, VCCI, osv. Vores virksomhed har et erfarent og professionelt teknisk ingeniørteam, som kan hjælpe virksomheder med at løse problemet. Hvis du har relevante test- og certificeringsbehov, kan du kontakte vores testpersonale direkte for at få detaljerede pristilbud og cyklusoplysninger!

FDA testrapport
Indlægstid: 21. august 2024